НОВОСТИ |
Важно знать в каких пропорциях разводить уксусную кислоту. Уксус горит или нет
www.ljpoisk.ru Температура вспышки уксусной кислоты - Справочник химика 21Постоянную А определяли по температуре вспышки уксусной кислоты. [c.26]Применяемая при производстве винилацетата уксусная кислота (СНзСООН) представляет собой горючую бесцветную жидкость с острым запахом и вкусом. Удельный вес ее 1,05. Кипит при 118°, застывает при 17°. Смешивается с водой. Кислота крепостью 99—99,5% (безводный уксус) носит название ледяной кислоты. Температура вспышки уксусной кислоты 38°. Верхний температурный предел взрываемости паров 60°. Температура самовоспламенения 500°. Пары уксусной кислоты В смеси с воздухом при концентрации от 3,1 до 12% взрывчаты. При нагревании до 300° разлагается с образованием ацетона. [c.76] Критическая температура составляет 321,6°С. Уксусная кислота смешивается во всех отношениях с этанолом, диэтиловым эфиром, бензолом и другими органическими растворителями и с водой. Растворяет некоторые неорганические и органические вещества, например, серу, фосфор, ацетаты целлюлозы. С воздухом уксусная кислота образует взрывчатые смеси с пределами воспламенения от 3,3 до 22,0% об. Температура вспышки равна 34°С, температура самовоспламенения 354°С. [c.309]Препарат не смачивается водой и индиферентен к кислотам и щелочам. До 400 °С не взаимодействует с Hj. Восстановление до графита происходит при кипячении с цинковой пылью и уксусной кислотой. Выше 400 °С начинается термическое разложение до летучих фторндов углерода, которое при быстром нагревании до более высоких температур сопровождается вспышками-и возгоранием. [c.677] Число омыления, мг КОН/г, не более Кислотность пересчете уксусную кислоту), КОН/100 см-, не более Температура вспышки, °С, не ниже Цветность по платинокобальтовой шкале, не более [c.159] Уксусная кислота (ледяная). Температура вспышки в закрытом тигле 42° С, температура самовоспламенения 428° С, температура кипения 118° С, пределы воспламенения 5,4— 16% (объемн.), раздражает кожу, глаза, дыхательные пути, токсична, в высокой степени взрывоопасна. При пожаре тушат распылением воды, углекислым газом, сухими порошками. Хранят в отдельных помещениях, предохраняют от механических повреждений. [c.181] При выборе места для расположения складов и их устройства учитывают горючесть и токсичность кислот. Кислоты с температурой вспышки до 120 °С следует хранить в соответствии с нормативными требованиями по хранению легковоспламеняющихся и горючих жидкостей. К таким кислотам относятся капроновая, муравьиная и уксусная с температурой вспышки соответственно 102, 60 и 38 °С. Большинство кислот — негорючие вещества. К сильнодействующим ядовитым веществам (СДЯВ) относятся дымящие кисло- [c.45] Уксусная кислота — легковоспламеняющаяся жидкость, имеющая температуру кипения 118,1 и температуру вспышки — 38 °С, плотность 1,049 т/м , температуру замерзания 16,7 °С. [c.58] Свойства. Бесцветная прозрачная. вязкая жидкость с рактерным арома-Температура плавления —8,6 X, температура кипения 223,3 °С. Плотность 1,184 г/см показатель преломления Вд" 1,536. Смешивается с этиловым спиртом, диэтиловым эфиром, хлоро- формом, ледяной уксусной кислотой, жирными и эфирными маслами, очень мало растворим в воде. Горюч, температура вспышки 99 С. Светочувствителен [c.226] Свойства. Бесцветная прозрачная подвижная жидкость с характерным, запахом. Плохо растворим в воде (1 2125 при 16 °С), смешивается с этиловым спиртом, диэтиловым эфиром, ацетоном, хлороформом, сероуглеродом, ледяной уксусной кислотой. Горюч. Легко воспламеняется. Температура вспышки 4Х . пары толуола с воздухом образуют взрывоопасные смеси. [c.391] Свойства. Бесцветная прозрачная сиропообразная гигроскопическая жид-кость, без запаха, сладкого вкуса. Смешивается с водой, спиртами, глицерином, уксусной кислотой, ацетоном и пиридином мало растворим в диэтиловом эфире, плохо растворим в углеводородах, жирах, сероуглероде. Горюч. Температура вспышки 120 С. Обладает наркотическими свойствами. [c.458] Производство кислородсодержащих соединений методом жидкофазного окисления ароматических углеводородов относится к числу взрыво- и пожароопасных вследствие применения легковоспламеняющихся и горючих веществ (уксусная кислота, метилацетат, метанол, алкилароматические углеводороды и др.), обладающих низкой температурой вспышки и высоким давлением насыщенных паров. Использование аппаратуры с большим объемом, работающей в условиях повышенных температур (до 220 °С) и давлений (до 3,0 МПа) с агрессивной рабочей средой создает повышенную взрыво- и пожароопасность. Применение в производствах токсичных и едких веществ (ароматические и алифатические карбоновые кислоты, щелочи, соединения галогенов и др.) создает опасность отравления персонала и появления химических ожогов. [c.230] Он является одним из многочисленных производных уксусной кислоты. Представляет собой бесцветную жидкость с резким запахом в 100 г воды при 15° С растворяется 2,7 г уксусного ангидрида, растворим в бензоле, эфире и хлороформе. Легко воспламеняется, температура вспышки 40° С, плотность 1,08 г/мл, температура кипения 140° С. [c.165] Принципиальная схема процесса переработки жижки с экстрагированием уксусной кислоты легкими растворителями показана на стр. 24—25 [24]. Подобным образом работает большая часть лесохимических предприятий Советского Союза. Но работа с этиловым эфиром осложняется взрывоопасностью (температура вспышки —40° С) и большой летучестью. Последнее обстоятельство приводит к необходимости охлаждения воды для сокращения потерь эфира при конденсации. [c.26] Кроме капролактама в расплавители в качестве стабилизаторов добавляют концентрированную уксусную кислоту, пары которой вызывают сильное раздражение слизистых оболочек. Для глаз опасны уже 2%-ные растворы уксусной кислоты, а 30%-ные растворы могут вызвать ожоги. Концентрированная уксусная кислота — легковоспламеняющаяся жидкость температура вспышки ее паров 38 °С, нижний предел воспламенения (взрываемости) 3,1% (об.), верхний — 22% (об.). [c.100] Предварительную обработ ку уксусной кислоты ведут обычно в особой емкости, снабженной деревянной мешалкой. Окислитель вносят малыми порциями (по 2— 3 кг) в увлажненном ввде, причем не допускают подъема температуры (за счет экзотермической реакции) выше 50 С во избежание вспышки паров уксусной кислоты. После внесения заданного количества окислителя содержимое куба перемешивают не менее часа, а затем отстоявшуюся уксусную кислоту передают в перегонный куб. [c.156] Е Ъ МЛ уксусного ангидрида постепенно растворяют 2 мл дымящей азотной кислоты (пл. 1,5) при охлаждении сосуда водой со льдом. Полученный раствор добавляют по каплям при перемешивании к охлаждаемому раствору, содержащему 2 г D-глюкозы в 5 лг уксусного ангидрида. Смесь оставляют на 15 мин при комнатной температуре, затем к ней добавляют безводный карбонат калия до нейтрализации кислоты. Смесь выливают в ледяную воду, твердый продукт отсасывают, промывают водой, перекристаллизовывают из небольшого количества горячего 95%-ного этилового спирта. Получается до 1,5 г белоснежного кристаллического вещества. (Осторожно При нагревании разлагается со вспышкой.) [c.84] Эти опыты показали также, что искра или раскаленная проволока не в состоянии вызвать взрыва этих ванн. Несмотря на это, если данные электролиты будут доведены до кипения или приведены в непосредственное соприкосновение с пламенем, вспышка возможна. Если они очень сильно нагреты (например, во время пожара), опасность взрыва особенно велика при больших объемах ванн. Данные опыты показали, что соблюдение определенных мер безопасности, и прежде всего в отношении температуры и предупреждения соприкосновения с открытым пламенем, снижает взрывоопасность, которая может быть еще более уменьшена заменой уксусного ангидрида его кислотой. [c.255] По другим данным, температура вспышки уксусной кислоты 38 С, а температура самово [c.748] Уксусный ангидрид (СНзС0)20 представляет бесцветную подвижную жидкость с резким запахом, с температурой кипения 139,9°С, температурой плавления -73,1°С и плотностью 1,08 т/м . Растворим в этаноле, диэтиловом эфире, бензоле, хлороформе, уксусной кислоте, холодной воде. В горячей воде гидролизуется до уксусной кислоты. Это необходимо учитывать при его производстве. Температура вспышки равна 40°С, температура самовоспламенения 389°С. Раздражает дыхательные пути и вызывает ожоги кожи. ПДК составляет 5-10 %. [c.310] Гексаи И трод И фен И Л представляет собой нейтральное стабильное вещество с температзроП плавлення 238— 240 и температурой вспышки 320°. Он почти не растворим в спирте, эфире, плохо растворим в кипящем бензоле, несколько легче в кипящей уксусной кислоте и кипящем толуоле. Гексаннтродифеиил несколько более чувствителен к удару, чем трнинтробензол, но меньше, чем тетрил. [c.150] Нитрозофениларсонивая кислота кристаллизуется в иглах, окрашенных в бледножелтый цвет. Хорошо растворима в горячей воде, плохо в холодной с образованием темнозеленых растворов. Кислота хорошо растворима в растворах едкой или углекислой щелочи, а также в уксусной кислоте. Плохо растворима или даже практически не растворима в метиловом спирте, этиловом спирте, эфире, хлороформе. Не плавится при нагревании до 180° продукт буреет и затем чернеет. При нагревании до высокой температуры наступает бурное разложение, сопровождающееся вспышкой. [c.183] Особенность схемы получения комплексных кальциевых смазок Бердянского НПЗ (рис.8) состоит в том, что она включает несколько периодических и непрерывных стадий. В нескольких контакторах-смесителях при 80-90°С периодически получают концентрат комплексного мыла, обрабатывая известью-пушонкой или известковым молоком смесь уксусной и синтетических жирных кислот с маслом [ИЗ. Промежуточная стадия-нагрев мыльно-масляно суспензии в трубчатом теплообменнике до 140°С, обезвоживание ее в скребковом роторном испарителе С12], работающем в пленочном режиме, нагрев до 225°С и охлаждение до температуры на 5-10°С ниже температуры вспышки масла, - осуществляется непрерывно. Подача антиокисли-тельной присадки производится попеременно в двух аппаратах, а охлаждение смазки до конечной температуры - непрерывно. [c.15] Свойства. Бесцветные кристаллы в виде игл или сплавленная белая кристаллическая масса с характерным запахом. Температура плавления 40,9 С, теМ пература кипения 182°С. На воздухе и свету постепенно краснеет. Растворим в воде (1 12,5 при 15°С), легко растворим в этиловом спирте, диэтиловом эфире, бензоле, хлороформе, ледяной уксусной кислоте и глицерине, практически не растворим в петролейном эфире. Возгоняется. С водой образует гидрат. Горюч, температура вспышки 75 X. Обжигает кожные покровы и действует на нербную систему. ПДК 5 мг/м . [c.411] Метилацетат (СН3СООСН3), или уксуснометиловый эфир, получается взаимодействием уксусной кислоты и метилового спирта. Это бесцветная легколетучая жидкость с ароматным запахом. Его удельный вес 0,93—0,94 легкая испаряемость метилацетата определяет низкую температуру кипения, которая равна+57,3. Пары метилацетата в 2,6 раза тяжелее воздуха. Метилацетат при очень низких температурах образует взрывоопасные смеси с воздухом, его температура вспышки равна — 15°. [c.18] Уксусная кислота является легковоспламеняющейся жидкостью. Температура вспышки ее паров равна 38°С. Температурные пределы воспламенения от 32°С (что соответствует нижнему концентрационному пределу 3,1%) до 60°С (соответствует верхнему концентрационному пределу 12%). Температура самовоспламенения 500°С, При горении уксусной кислоты выделяется 3490 ккал1к2. [c.140] Адипиновая кислота [НООС(СНг)4СООН] представляет собой кристаллический порошок, температура плавления которого равна 153°С. Удельный вес 1,36 г/см . При температуре 330°С кипит с разложением. Растворяется в воде, спиртах, уксусной кислоте. Не ядовита. Адипиновая кислота — горючее вещество. Температура вспышки равна 196°С. Горит бесцветным пламенем. Па1ры в смеси с воздухом образуют взрывоопасные концентрации в пределах 3,5—8% (по объему). [c.140] Уксусная кислота СНзСООН — бесцветная легковоспламеняющаяся жидкость с характерным запахом. Плотность жидкости при 20 °С 1,049 плотность па])ов по воздуху (при О °С и 760 м.ч рт. ст.) 2,07. Температура кипения 118,1 °С, плавления 16,7 °С, вспышки 38,0 °С, самовоспла.менения 454 °С. Пределы взрываемости в смеси с воздухом (объемн. %) нижиий — 3,1, верхний — 12,0. Уксусная кислота растворяется в этаноле, этиловом эфире и др. В воде растворяется в люб1лх соотношениях. Средства пожаротушения — распыленная вода, газовые и порошковые составы. Кислота вызывает ожоги кожи пары действуют раздражающе па слизистые оболочки и верхние дыхательные путл. Предельно допустимая концентрация в воздухе нроизводствеииых помещений 5 мг/.ч К Средство индивидуальной защиты — противогаз с коробкой марки В. [c.123] Масляная кислота С3Н7СООН (мол. масса 88,104) -бесцветная маслянистая жидкость с едким запахом, напоминающим запах уксусной кислоты и прогорклого масла, с кислым жгучим вкусом. Застывает при -7,9°С, кипит при 163,5°С. Плотность жидкости при 0° 0,978, при 15°С 0,963, при 25° 0,953 г/см. Температура вспышки 76,7°С. [c.70] Диэтилфталат—бесцветная, прозрачная жихкость с температурой кипения 295°, удельным весом 1,П79, температурой вспышки 40 и температурой воспламенения 170° С число омыления 503, показатель преломления 1,501, летучесть (погеря, в после 6-часового пребывания при 100° С) 6,59, кислотное число (рассчитанное на уксусную кислоту) 0,015, содержание воды в % (растворимость в 7[c.311] Эфир окисляется хромовс й кислотой в уксусную и так сильно, что происходит вспышка или даже взрыв. Азотная кислота разлагает его, образуя уксусную, щавелевую и угольную кислоты.- Две последние суть, вероятно, побочные продукты. Хлор отнимает водород у эфира, превращая его радикал в ацетил. При пропускании паров эфира чрез разогретое едкое кали с известью происходит, по Дюма и Штассу, совершенное разложение на неорганические продукты, и получаются углекислота, водород и болотный газ. Вероятно, лри этом последнем опыте температура была слишком высока, иначе тру но предположить, чтоб не было образования [c.484] chem21.info Уксусная кислота: свойства и все характеристикиХарактеристики и физические свойства уксусной кислотыПри попадании на слизистые оболочки она вызывает ожоги. Уксусная кислота смешивается с водой в любых соотношениях. Образует азеотропные смеси с бензолом и бутилацетатом. Уксусная кислота замерзает при 16oС, её кристаллы по внешнему виду напоминают лед, поэтому 100%-ную уксусную кислоту называют «ледяной». Некоторые физические свойства уксусной кислоты приведены в таблице ниже:
Получение уксусной кислотыВ промышленности уксусную кислоту получают каталитическим окислением н-бутана кислородом воздуха: Ch4-Ch3-Ch3-Ch4+ [O2] = 2Ch4-COOH. Значительные количества уксусной кислоты производят путем окисления ацетальдегида, который в свою очередь получают окислением этилена кислородом воздуха на палладиевом катализаторе: Ch3=Ch3 + [O2] = Ch4-COH + [O2] =Ch4-COOH. Пищевую уксусную кислоту получают при микробиологическом окислении этанола (уксуснокислое брожение). При окислении бутена-2 перманганатом калия в кислой среде или хромовой смесью происходит полный разрыв двойной связи с образованием двух молекул уксусной кислоты: Ch4-CH=CH-Ch4 + [O2] = 2Ch4-COOH. Химические свойства уксусной кислотыУксусная кислота – это слабая одноосновная кислота. В водном растворе она диссоциирует на ионы: Ch4COOH↔H+ + Ch4COOH. Уксусная кислота обладает слабыми кислотными свойствами, которые связаны со способностью атома водорода карбоксильной группы отщепляться в виде протона. Ch3COOH + NaOH = Ch4COONa + h3O. Взаимодействие уксусной кислоты со спиртами протекает по механизму нуклеофильного замещения. В качестве нуклеофила выступает молекула спирта, атакующая атом углерода карбоксильной группы уксусной кислоты, несущий частично положительный заряд. Отличительной особенностью этой реакции (этерификации) является то, что замещение протекает у атома углерода, находящегося в состоянии sp3-гибридизации: Ch4-COOH + Ch4OH = Ch4O-C(O)-Ch4 + h3O. При взаимодействиистионилхлоридом уксусная кислота способна образовывать галогенангидриды: Ch4-COOH + SOCl2 = Ch4-C(O)Cl + SO2↑ + HCl↑. При действии на уксусную кислоту оксида фосфора (V) образуется ангидрид: 2Ch4-COOH + P2O5 = Ch4-C(O)-O-C(O)-Ch4 + 2HPO3. Взаимодействии уксусной кислоты с аммиаком получаются амиды. Вначале образуются аммониевые соли, которые при нагревании теряют воду и превращаются в амиды: Ch4-COOH + Nh4↔Ch4-COO—Nh5+↔Ch4-C(O)-Nh3 + h3O. Применение уксусной кислотыУксусная кислота известна с глубокой древности, её 3 – 6% растворы (столовый уксус) используют как вкусовую приправу и консервант. Консервирующее действие уксусной кислоты связано с тем, что создаваемая ею кислая среда подавляет развитие гнилостных бактерий и плесневых грибков. Примеры решения задачru.solverbook.com Уксусная кислота – свойства, области применения, пищевая добавка Е-260Одной из первых кислот, которая стала известна людям еще в древности, стала уксусная кислота. Обнаружено это было случайно – вследствие появления уксуса при скисании вина. В 1700 году Шталь получил концентрированную разновидность химической разновидности жидкости, а в 1814 – Берцелиус установил точный его состав. Получение уксусной кислоты возможно разными путями, а применяется она достаточно широко во многих направлениях хозяйственной деятельности. Что такое уксусная кислота?Уксусная кислота является синтетическим продуктом брожения углеводов и спиртов, а также естественного скисания сухих виноградных вин. Принимая участие в процессе обмена веществ в организме человека, данная кислота является пищевой добавкой, используемой для приготовления маринадов и консервации. Производными кислоты считаются уксус – 3-9%, и уксусная эссенция – 70-80%. Эфиры и соли уксусной кислоты называются ацетатами. В состав обычного уксуса, к которому привыкла каждая хозяйка, входит аскорбиновая, молочная, яблочная, уксусная кислоты. Ежегодно в мире производится почти 5 миллионов тонн уксусной кислоты.
Транспортировка кислоты на разные расстояния осуществляется в железнодорожных или автомобильных цистернах, изготовленных из специализированных марок нержавеющей стали. В складских условиях она хранится в герметичных емкостях, контейнерах, бочках под навесами или в помещениях. Заливать и хранить вещество в полимерной таре можно в течение одного календарного месяца. Качественные характеристики уксусной кислотыБесцветная жидкость с кислым привкусом и резковатым запахом, которой является уксусная кислота, имеет ряд определенных преимуществ. Конкретные свойства делают кислоту незаменимой во многих химических соединениях и продуктах бытового назначения.
Уксусная кислота, как одна из представителей карбоновых, имеет способность к проявлению высокой реакционной способности. Вступая с самыми разными веществами в реакции, кислота становится инициатором соединений с функциональными производными. Благодаря подобным реакциям, становится возможным:
К уксусной кислоте предъявляется ряд определенных технических требований. Жидкость должна растворяться в воде, не иметь механических примесей и иметь установленные пропорции качественных составляющих. Основные области применения уксусной кислоты Е-260Разнообразие сфер, в которых применима уксусная кислота, достаточно велико. Данная кислота является непременным компонентом многих лекарственных препаратов – например, фенацетина, аспирина и других разновидностей. Ароматические амины Nh3-группы защищаются в процессе нитрования введением ацетильной группы СН3СО – это также одна из наиболее распространенных реакций, в которые вступает уксусная кислота. Довольно важную роль играет вещество при изготовлении ацетилцеллюлозы, ацетона, различных синтетических красителей. Не обходится без ее участия производство разнообразной парфюмерии и негорючих пленок.
Часто применима уксусная кислота в пищевой промышленности – в качестве пищевой добавки Е-260. Консервирование и бытовая кулинария также являются успешным полем действия и применения качественной натуральной добавки. При крашении основные типы солей уксусной кислоты играют роли специальных протрав, обеспечивая стабильную связь текстильных волокон с красителем. Эти соли часто применяются в борьбе с самыми стойкими разновидностями растений-вредителей. Меры предосторожности при работе с уксусной кислотойУксусная кислота считается легковоспламеняющейся жидкостью, которой присвоен третий класс опасности – в соответствии с классификацией веществ по степени опасного воздействия на организм. При любых работах с данным видом кислоты специалисты пользуются индивидуальными современными средствами защиты (фильтрующими противогазами).
Даже пищевая добавка Е-260 может оказаться токсичной для человеческого организма, однако зависеть степень воздействия будет от качества разбавления водой концентрированной уксусной кислоты. Растворы, концентрация кислоты в которых превышает уровень в 30%, считаются опасными для жизни. Соприкасаясь с кожей и слизистыми оболочками, уксусная кислота высокой концентрации вызовет сильнейшие химические ожоги. При этом способ получения кислоты не играет особой роли в ее токсикологической направленности, а смертельной может быть доза от 20 мл. Различные последствия могут стать губительными для многих человеческих органов – начиная от ротовых слизистых и дыхательных путей и заканчивая желудком и пищеводом. При неосторожном попадании кислоты внутрь важно пить как можно больше жидкости до приезда медиков, но ни в коем случае не вызывать рвоту. Повторное прохождение веществ по организму может повторно обжечь органы. В дальнейшем необходимым будет промывание желудка при помощи зонда и госпитализация. www.sciencedebate2008.com Уксус и уксусная кислота: сходства и различияСтоловый уксус – продукт, известный человечеству с давних времен. Уже в III веке до нашей эры люди пользовались уксусом для различных целей. Уксус был непременным компонентом для консервации продуктов (особенно актуально при отсутствии холодильных агрегатов), с его помощью получали различные красящие вещества и так далее. Уксус широко используется и в настоящее время. На любой кухне можно отыскать бутылочку с уксусом, особенно, если хозяйка увлекается консервированием. Но такое широкое распространение уксуса иногда приводит к отравлениям – уксус путают с уксусной кислотой, что и является главной причиной несчастных случаев. Рассмотрим же сходства и различия уксуса и уксусной кислоты. Что такое уксусная кислотаУксусную кислоту еще называют этановой кислотой, и ее химическая формула СН3СООН. В древние времена уксусную кислоту получали путем брожения виноградного вина или других продуктов (к примеру, яблочного сока). Во времена Возрождения для получения уксусной кислоты использовали ацетаты металлов. Интересно, что свойства этой кислоты изменяются в зависимости от растворения, то есть, водные растворы уксусной кислоты разной процентности показывают различные свойства и качества. По этой причине химики очень долго считали, что кислота, произведенная с помощью ацетатов металлов, является другим веществом, нежели та, что получена из органических веществ (из вина или сока). Лишь в XVI столетии было доказано, что вне зависимости от способа получения это все та же уксусная кислота.
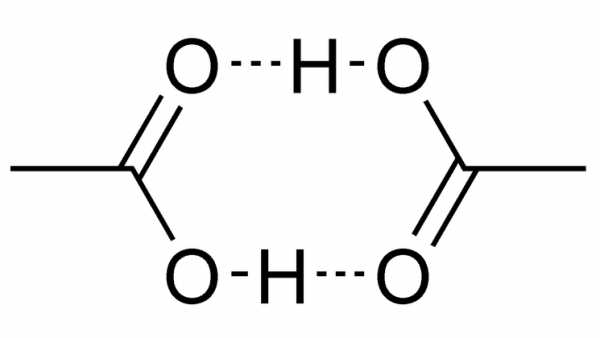
В XIX столетии уксусная кислота была получена путем синтеза неорганических веществ: в качестве исходного сырья использовался сероуглерод. Уксусная кислота в обычных условиях является водным раствором с концентрацией 80%. Существует также безводная или ледяная уксусная кислота – по внешнему виду она напоминает лед, отсюда и название. Концентрация такой кислоты составляет 99-100%. Еще производится уксусный ангидрид, но он используется в фармацевтической промышленности (синтез аспирина).
Как и любая концентрированная кислота, уксусная кислота представляет собой опасность. Известны случаи, когда люди по ошибке выпивали уксусную кислоту, и это приводило к ожогам слизистой оболочки носоглотки, желудка и пищевода, а химические ожоги считаются самыми тяжелыми даже если речь идет об ожоге кожи, что уж говорить о внутренних органах. Кроме того, прием внутрь уксусной кислоты вызывает и другие осложнения, к примеру, нарушение свертываемости крови, шок и так далее. Поэтому если вы держите дома уксусную кислоту, то необходимо, чтобы она находилась вне доступа детей, а также хранилась в такой таре, которую невозможно перепутать с какой-либо безобидной жидкостью. ВНИМАНИЕ! Летальный исход наступает при употреблении уксусной кислоты от 20 мл и более! Что такое уксусУксус имеет ту же химическую формулу, что и уксусная кислота, и представляет собой то же химическое соединение. Единственное отличие уксуса от уксусной кислоты заключается в том, что обычная уксусная кислота является концентрированным уксусным раствором (около 80%), а уксус – сильный водный раствор, и его концентрация составляет 6-9%.
Уксусная кислота используется в основном в производстве, а в бытовых условиях применяется ее слабый раствор, который мы называем столовым уксусом. Уксус используется для консервации продуктов, а в некоторых случаях и в качестве жаропонижающего. Следует заметить, что жаропонижающим средством уксус служит не при внутреннем, а только при наружном употреблении – его применяют для растираний при высокой температуре, а также смачивают уксусом примочки (в этом случае примочка дольше сохраняется прохладной).
Необходимо знать, что уксусная кислота раздражает слизистую оболочку носоглотки, особенно сильно ее воздействие при нагреве, а ведь часто при консервации в бытовых условиях приходится готовить маринад, добавляя уксус в кипящую воду. Поэтому требуется, чтобы помещение, где осуществляется домашняя консервация продуктов, хорошо проветривалось. Также не рекомендуется находиться в помещении во время консервирования людям, страдающим легочными заболеваниями. Получаем уксус из концентратаВ «закаточный сезон», когда все хозяйки бросаются консервировать овощи на зиму, случается, что в магазинах пропадает обычный столовый уксус, зато продается уксусная эссенция. Если вы не собираетесь удалять накипь с чайника или кастрюль (а уксусная кислота превосходно справляется с этой задачей), то эссенцию можно легко превратить в обычный уксус, а после этого использовать для консервации продуктов. Для того, чтобы уксусная кислота стала уксусом, нужно всего лишь добавить в нее воды. vchemraznica.ru Ответы@Mail.Ru: Вода, перекись водорода, соль, уксус- всё взболтатьОчарованы зрелищем светящихся в темноте предметов или жидкостей в стакане? Непременно хотите знать, как сделать светящуюся жидкость своими руками? Ну что ж, придется разбираться. Только учтите, что изготовление светящейся жидкости в домашних условиях не самое простоя, а главное не очень чистое, так что посуду после опытов мыть вам придется. Как сделать светящуюся жидкость своими руками? Понятно, что жидкость светится в темноте не просто так, видимо какие-то химические процессы происходят. Углубляться в химию не будем, просто примем как данность, что некоторые вещества в кислой среде начинают излучать свет. Поэтому чтобы все нужные произошли нужно заготовить необходимые реагенты. Рецепт светящейся жидкости существует не один, поэтому рассмотрим несколько способов ее приготовления. Способ 1 Вам потребуется: люминол (продается в магазинах, торгующих химреактивами) – 2-3 г; перекись водорода 3% (из аптеки) – 80 мл; вода – 100 мл; медный купорос (хлорное железо, красная кровяная соль) – 3 г; раствор едкого натра – 10 мл; флуоресцентные красители – рубрен, бриллиантовый зеленый и т. д. пробирки (колбы, прозрачные стеклянные емкости) . Изготовление Люминол порошок желтого цвета, который в кислых и нейтральных растворах начинает светиться голубым цветом. Так что не зря он стоит в рецепте на первом месте, без люминола опыт не удастся. Наливаем в колбу воду, растворяем в ней люминол. Добавляем в колбу перекись водорода. Туда же отправляем медный купорос или хлорное железо, или красную кровяную соль. Если не нашлось ни того, ни другого, ни третьего, можно обойтись подручными средствами. Выдавливаем из куриного окорочка немного крови, разводим ее в воде и добавляем 1 ст. ложку этого раствора к смеси в колбе. Добавляем в колбу едкий натр. Выключаем свет и любуемся на дивное голубое свечение, исходящее от колбы. Если голубой цвет вам не по нутру (есть такие люди) , то добавляем к раствору в колбе любой флуоресцентный краситель. Способ 2 Вам потребуется: люминол – 0,15 г; сухая щелочь (КОН) – 35 г; димексид (диметилсульфоксид) – 30 мл; колба с пробкой объемом 500 мл; флуоресцентный краситель. Изготовление Смешиваем в колбе люминол, щелочь и димексид. Закрываем колбу крышкой и встряхиваем. Появится свечение голубого цвета, которое можно перекрасить, добавив к составу любой флуоресцентный краситель. Если свечение ослабло, открываем крышку, впускаем в колбу немного воздуха. И вот жидкость снова стала излучать свет. Способ 3 Вам потребуется: высокий стакан – 1 шт. ; раствор стирального порошка – 20 мл; перекись водорода 3% - 10 мл; раствор люминола 3% - 5 мл; несколько кристаллов марганцовки. Изготовление Наливаем в стакан раствор стирального порошка. Туда же отправляем перекись водорода и раствор люминола. Отдельно растираем несколько кристаллов перманганата калия (марганцовки) и тоже отправляем в стакан. При попытке перемешать, смесь вспенится, и будет красиво искриться. Но, как уже говорилось выше, после всех опытов придется дома прибраться и вымыть посуду. Но и этот процесс можно сделать увлекательным, если притенить комнату. Под воздействием хлорированной водопроводной воды растворы люминола начнут светиться. Как сделать люминофор? Как делать светящуюся жидкость теперь понятно, но если кто-то хочет пойти по пути химика-испытателя чуть дальше, то можно попробовать изготовить люминофор самостоятельно. Для этого приобретем в аптеке хвойный концентрат и борную кислоту. Растворяем 1 грамм хвойного концентрата в воде. Берем ложку и кладем на нее немного борной кислоты. По капле в ложку добавляем раствор хвойного концентрата и аккуратно перемешиваем. Кипятим над огнем, пока в ложке раствор не закипит, пузыри прокалываем чем-нибудь острым. Охлаждаем, добавляем еще раствора и снова прогреваем состав. Получится желтое вещество – люминофор. После пребывания на ярком свету (можно использовать вспышку) будет светиться в темноте, но недолго, несколько секунд. Для создания светящейся жидкости вам потребуется: четыре чайных ложки перекиси водорода – лучше взять 3%; две столовые ложки соли пищевой; четыре столовых ложки уксуса; примерно 500 мл воды. 2 наталья мерзук получиться раствор для травления печатных плат :) У меня не получилось у меня тоже ожет краску над добавлять не получилось серьезно??? и не получится вообще -__- Попробуй этот способ !!!1. Возьмите стакан и налейте туда воды. Затем насыпьте в воду 1 ч. ложку соды. 2. Далее возьмите перекись водорода, откройте и используя крышку от пузырька в качестве мерки влейте в стакан 2 крышечки перекиси и размешайте. 3. Теперь опустите в получившийся раствор шнурки и подержите 5 минут, затем выньте и дайте им просохнуть. Вот и все, светящиеся шнурки готовы. XD XD xD вы йойо нутые touch.otvet.mail.ru Во избежание несчастных случаев в быту необходимо знать, как правильно разбавить уксусную кислотуУксус – это продукт брожения вина, который известен человеку с очень давних времен. Впервые данное вещество применяли в третьем веке до нашей эры. Известный грецкий ученый Теофраст первым описал воздействие уксуса на металлы, приводящее к появлению некоторых пигментов, используемых в искусстве. Еще в Древнем Риме готовили специально вино в свинцовых горшках. Такое вино было очень прокисшее, что и являлось его отличительной особенностью. В результате получался напиток повышенной сладости, который имел название «сапа». «Сапа» в своем составе содержала очень много ацетата свинца – того самого сладкого вещества. Из-за этого напитка в римской аристократии было очень распространено свинцовое отравление. В начале VIII века Джабирибн Хайян – арабский алхимик, впервые смог получить уксусную кислоту посредством перегонки. Уксусная кислота – это бесцветная жидкость с характерным для нее кислым вкусом и резким запахом. Она гигроскопична. В воде растворяется в неограниченных пределах, поэтому следует наперед знать в каких пропорциях разводить уксусную кислоту. Она способна смешиваться с большинством растворителей, но лучше всего с HCl, HF, HBr, HI. Существует в виде линейных и циклических димеров. Как получают уксусную кислоту?Одним из наиболее распространенных промышленных способов получения уксусной кислоты является окисление ацетальдегида кислородом воздуха. Процесс выполняется в присутствии специального катализатора – ацетата марганца при температуре от 50 до 60 °С. 2Ch4CHO + O2 → 2 Ch4COOH Ранее использовались другие методы получения уксусной кислоты, такие как окисление бутана и ацетальдегида. Окисление ацетальдегида происходило в присутствии марганца при повышенном давлении и температуре. На выходе можно было получить 95% уксусной кислоты.
Но все же натуральная кислота – это та, которая получается путем брожения. Это может быть виноградное или яблочное вино. Свойства данного вещества могут изменяться в зависимости от процентного содержания в ней воды. Из-за этого много веков химики считали, что кислота из ацетатов, и кислота из вина – это два разных вещества. Естественно это мнение было ошибочным. Все зависит от концентрации воды. Виды уксусной кислоты.96-100% - это ледяная (безводная) уксусная кислота, представляющая собой бесцветную гигроскопическую жидкость или же бесцветные кристаллы с очень неприятным и резким запахом. Ледяная уксусная кислота используется для реализации синтеза различных красителей, а также для ускоренного получения ацетона и ацетата целлюлозы. Ледяная кислота может использовать и в пищевой промышленности, но только в виде уксусной эссенции или уксуса. Следует отметить, что в быту ее можно использовать для приготовления пищи. Это связано с тем, что ее можно легко разбавить с водой, зная правильные пропорции. Ледяную уксусную кислоту получают путем синтеза, либо брожением нескольких органических веществ. Также ледяная кислота всегда содержится в продуктах сухой перегонки определенных сортов дерева. 70-80% раствор уксусной кислоты называется уксусной эссенцией. Уксусная эссенция – это торговое название водного раствора пищевой уксусной кислоты, которую получают брожением уксуснокислых спиртовых жидкостей. Как правило, уксусная эссенция используется в процессе приготовления маринадов, столового уксуса и консервирования продуктов. Бывают случаи, когда в рецепте для закрутки нужна уксусная эссенция, а на кухне есть только обычный столовый 9% уксус, или наоборот. Большинство хозяек не знают, как выйти из этого положения. Поэтому следует знать, что данные жидкости взаимозаменяемые. Главное знать, как правильно разбавить уксусную кислоту, а именно в каких пропорциях. Например, из столового уксуса необходимо получить 70% раствор уксусной эссенции. При этом нужно уменьшать количество воды на столько, сколько предусматривается добавлять укуса. Формула расчета очень простая: 1 столовая ложка уксусной эссенции = 8 столовым ложкам уксуса 9% на 7 столовых ложек воды; 1 столовая ложка уксусной эссенции = 12 столовым ложкам уксуса 6% на 11 столовых ложек воды; 1 столовая ложка уксусной эссенции = 21 столовая ложка уксуса 3% на 20 столовых ложек воды. Следует отметить, что уксусная эссенция – это довольно токсичное вещество, отравление которым считается наиболее частым из бытовых интоксикаций. Так, смертельная доза, при отсутствии сверенной медицинской помощи составляет 30-50 миллилитров 80% уксусной эссенции. Если кто-то выпил уксусную кислоту в чистом виде, то его ждут тяжелые ожоги слизистых оболочек глотки и полости рта, а также поражается желудок и пищевод. К наиболее распространенным последствиям всасывания уксусной кислоты относятся гемолиз, гемоглобинурия, ацидоз, а также нарушение свертываемости крови. Уксус (3-15% водный раствор уксусной кислоты) – продукт с определенным содержанием уксусной кислоты. Зачастую данное вещество получают в результате микробиологического синтеза при помощи уксуснокислых бактерий из специального спиртосодержащего сырья. Также столовый уксус можно получить из ледяной уксусной кислоты или укосной эссенции, нужно только знать, как разводится уксусная кислота. Это слабо окрашенная или бесцветная прозрачная жидкость с резким кислым вкусом и специфическим неприятным ароматом. Уксус подразделяют на синтетический и натуральный. Он широко используется в кулинарии. Пищевой уксус натурального типа вырабатывается в таком ассортименте: Фруктовый и яблочный (из плодового сырья). Спиртовой (из этилового спирта для пищевого производства). Винный (из винограда и виноматериалов). Бальзамический (из винограда и виноматериалов путем длительного выдерживания в бочках из различных пород дерева). Ароматизированный спиртовой с натуральными ароматизаторами (экстрактами растений, специями). Солодовый. Сывороточный (из очищенной молочной сыворотки). Что касается синтетического уксуса, то для пищевых целей его выпускают в чистом виде и с добавлением различных ароматизаторов (синтетических, идентичных натуральным и натуральных). Следует отметить, что в некоторых странах запрещено производство уксуса для пищевых целей (Болгария, США и Франция). Разбавляем уксусную эссенцию правильно.Уксус является незаменимым помощником в быту, а именно на кухне. Существует уксус различной концентрации, но наиболее часто хозяйки используют укус 6% и 9% концентрации. Уксусную эссенцию не используют по причине незнания или неумения того, как приготовить 3 раствор уксусной кислоты, имея при этом 70% эссенцию.
На сегодняшний день на бутылках с этикетками уксусной эссенции производители пишут, что ее нужно разбавить с водой в соотношении 1:20, но это не совсем верно. Также существуют бутылки, где такой надписи вовсе нет. Поэтому нужно знать, как использовать уксусную эссенцию, чтобы получить столовый укус различной концентрации. Для разведения эссенции нужно взять холодную воду, отфильтрованную или кипяченую. За условную единицу (1 часть) можно считать 1 столовую ложку. Расчет на калькуляторе для уксуса покажет обратное соотношение уксусной эссенции к столовому уксусу. Чтобы приготовить 3% уксус, нужно взять 1 часть уксусной эссенции и разбавить ее в 22 или 22,5 частях воды, то есть получается соотношения 1:22 или 1:22,5. Если рассчитывать на специальном калькуляторе для уксуса, то вместо 1 столовой ложки, которая содержит 15 мл жидкости, 70%-ного уксуса необходимо взять 24,9 столовых ложки 3% уксуса. Для приготовления 4%-ного уксуса следует взять 1 часть эссенции и разбавить ее в 17 частях воды. Получается соотношение 1:17. Из расчета на специальном калькуляторе для уксуса показатели следующие: вместо 1 столовой ложки 70%-ного уксуса следует взять 18,6 столовых ложек 4%-ного столового уксуса. Если нужно приготовить 5%-ный уксус, тогда соотношение будет 1:13, то есть одну часть уксусной эссенции необходимо разбавить в 13 частях воды. Рассмотрев расчет на калькуляторе для укуса покажет, что вместо одной столовой ложки 70%-ного уксуса следует взять 14,9 столовых ложки столового уксуса с концентрацией 5%. Если вы не знаете, как развести уксусную кислоту до 6 уксуса, тогда нужно взять одну часть уксусной эссенции и разбавить ее в 11 частях воды, то есть в соотношении 1:11. Расчет на калькуляторе для уксуса покажет, что вместо одной столовой ложки уксусной эссенции необходимо взять 12,4 столовых ложки уксуса 6%. Для приготовления 7%-ного столового уксуса из уксусной эссенции следует взять одну часть эссенции и разбавить ее в 9 частях воды (соотношение 1:9). Обратный расчет на калькуляторе покажет, что вместо одной столовой ложки 70%-ной уксусной кислоты необходимо взять 10,6 столовых ложек уксуса с концентраций 7%. Чтобы приготовить столовый уксус с концентрацией 8% нужно взять одну часть уксусной эссенции и разбавить ее в соотношении 1:8, то есть в 8 частях воды. Расчет на калькуляторе для уксуса покажет, что вместо одной столовой ложки 70%-ного уксуса следует взять 9,3 столовых ложки уксуса 8%-ного. Перед тем как развести уксусную кислоту до 9 процентного уксуса, нужно удостовериться, что эссенция имеет концентрацию 70%. После этого одну часть уксусной эссенции следует разбавить в 7 частях воды (соотношение 1:7). Расчет на калькуляторе покажет, что вместо одной столовой ложки эссенции с концентраций 70% необходимо взять 8,2 столовых ложек 9%-ного столового уксуса. Чтобы приготовить 10%-ный столовый уксус, берется одна часть уксусной эссенции и разбавляется в соотношении 1:6, то есть в 6 частях воды. Из расчета на «уксусном» калькуляторе будет видно, что вместо одной столовой ложки 70%-ного уксуса следует взять 7,4 столовых ложки уксуса с концентрацией 10%. Для приготовления 30%-ного уксуса, что бывает очень необходимо в случае консервирования различных овощей, нужно одну часть эссенции разбавить в 1,5 частях воды, то есть в соотношении 1:1,5. Расчет на калькуляторе для уксуса покажет, что вместо одной столовой ложки 70%-ного уксуса следует взять 2,4 столовых ложки уксуса с концентрацией 30%. Бывают случаи, когда вместо 70%-ного уксуса люди по ошибке покупают 30%-ный. Но это не проблема, поскольку его также можно легко разбавить, только нужно знать, как правильно развести укосную кислоту с концентраций 30%, поскольку пропорции уже будут другими. Для того, чтобы из уксусной эссенции, которая имеет концентрацию 30% получить обычный 3%-ный столовый уксус нужно ее разбавить в соотношении 1:10. То есть одна часть уксусной эссенции разбавляется в 10 частях воды. Обратный расчет на калькуляторе для укуса покажет, что вместо одной столовой ложки 30%-ного уксуса следует взять 1,4 столовых ложки столового уксуса с концентраций 3%. Для приготовления 4%-ного столового укуса из уксусной эссенции с концентрацией 30% нужно одну ее часть разбавить в 7 частях воды, то есть в соотношении 1:7. Если произвести расчет на специальном калькуляторе для укуса, то он покажет, что вместо одной столовой ложки 30%-ного уксуса следует взять 7,8 столовых ложек обычного 4%-ного уксуса. Чтобы приготовить столовый уксус с концентрацией 5% следует разбавить одну часть 30%-ной уксусной эссенции в 6 частях воды (соотношение 1:6). Выполнив расчет на калькуляторе для уксуса можно удостовериться, что вместо одной столовой ложки 30%-ного укуса необходимо взять 6,2 столовых ложки укуса с концентрацией 5%. Если вы не знаете, как сделать из уксусной кислоты 6 уксус, тогда вам нужно взять одну часть уксусной эссенции с концентраций 30% и разбавить ее в 5 частях холодной, инфильтрированной воды, то есть в соотношении 1:5. Обратный расчет на специальном калькуляторе для укуса покажет, что вместо одной части эссенции необходимо взять 5,2 столовых ложки обычного столового уксуса с концентрацией 6%. В ходе приготовления столового уксуса с концентрацией 7%, по сути ничего не меняется кроме пропорции. Следует взять одну часть 30%-ной уксусной эссенции и разбавить ее в 4 частях воды. Расчет на «уксусном» калькуляторе покажет, что вместо 1 столовой ложки 30%-ного уксуса следует взять 4,4 столовых ложки 7%-ного столового уксуса. Чтобы приготовить из уксусной эссенции с концентрацией 30% обычный 8%-ный столовый уксус нужно взять одну часть эссенции и разбавить ее в 3,5 частях воды. Соотношение будет 1:3,5. Из расчета на специальном калькуляторе для укуса покажет, что вместо одной столовой ложки укуса с концентрацией 30% следует взять 3,9 столовых ложки обычного 8%-ного столового уксуса. Перед тем как перевести уксусною кислоту в уксус 9 следует заранее подготовить холодную отфильтрованную воду и проверить имеет ли уксусная эссенция концентрацию 30%, поскольку ниже будет представлено соотношение именно для этой концентрации. Одну 30%-ной уксусной кислоты нужно разбавить в 3 частях воды. Если рассмотреть расчет на калькуляторе для уксуса, то вместо одной столовой ложки уксуса с концентрацией 30% следует взять 3,4 ложки обычного 9%-ного уксуса. Для приготовления 10%-ного уксуса из уксусной эссенции с концентрацией 30% нужно взять одну ее часть и разбавить в 2,5 частях воды (соотношение 1:2,5). Расчет на калькуляторе для уксуса покажет, что вместо одной столовой ложки 30%-ного уксуса необходимо взять 3,1 столовых ложки обычного столового уксуса с концентрацией 10%. Итак, выше были рассмотрены наиболее распространенные соотношения получения уксуса определенной концентрации. Но вы всегда можете сами добиться нужной концентрации, для этого следует знать одну небольшую формулу: K = Сисх/Стр. В этой формуле К – это коэффициент, Сисх – исходная концентрация, Стр – требуемая концентрация. Чтобы эту формулу было проще понять рассмотрим небольшой пример. Нам нужно разбавить 70%-ную уксусную эссенцию, так, чтобы получить столовый уксус с концентраций 2%. Подставляем значения в формулу: К = 70/2 = 35. Таким образом, чтобы получить 2%-ный уксус, нужно 1 часть эссенции развести 35 частями воды. Техника безопасности при работе с уксусной эссенцией.Уксусная эссенция или в разбавленный пищевой уксус очень часто являются виновниками ожогов и отравления. Наиболее часто вызывает отравление и ожоги именно уксусная эссенция с концентрацией 70%. Это происходит по причине того, что большинство людей не знают, как перевести уксусную кислоту в укус 9 и делают это «на глаз». Не только 70%-ная уксусная кислота может вызвать ожоги и отравление, этого можно добиться и 30%-ной кислотой. Даже укус с концентрацией 2% является опасным, для глаз особенно. Если уксусная эссенция была принята внутрь, то сразу же во рту, глоте и по ходе всего пищеварительного тракта образуется ожог, вызывающий резкую боль. Боль будет продолжаться при глотании и продолжается около 10 дней. Ожог желудка, кроме боли, сопровождается рвотой с кровью. Попадая в гортань, уксусная эссенция вызывает осиплость голоса и оттек, который может привести к затруднению дыхания, свистящему дыханию, посинению кожи и удушью. Если внутрь было принято 15-30 мл жидкости – это вызывает легкую форму отравления, 30-70 мл – среднюю, а 70 мл и выше – тяжелую, при которой вероятен смертельный исход. В большинстве случаев смерть наступает на первые сутки после отравления из-за болевого шока, гемолиза и других явлений интоксикации. На вторые-пятые сутки после отравления смерть вызывает пневмония, а в более отдаленные сроки обильное кровотечение из пищеварительного тракта. В случае острого отравления, причинами смерти являются острая печеночная и почечная недостаточность. Поэтому следует запомнить такие правила: - не выполнять чистку монет уксусной эссенцией на кухне; - выполняя чистку монет, одновременно не пить напитки и не есть пищу; - тщательно мыть руки, если они были запачканы в растворе. Первая помощь при отравлении уксусом или уксусной эссенцией.Если вы неправильно выполнили разбавление уксусной кислоты, или каким-либо другим способом отравились уксусной кислотой, тогда нужно неотложно прибегать к первой помощи. В случае попадания в глаза, их нужно немедленно, обильно и длительно промывать их холодной водой, после этого закапать 1-2 капли новокаина. После этого нужно капать специальные антибиотики, например, 0,25%-ный раствор левомицетина. Раздражение верхних дыхательных путей устраняется полосканием горла и носа холодной водой, ингаляцией раствором соды. Также рекомендуется пить теплую воду боржоми или молоко с содой. В случае попадания на кожу, ее нужно тщательно промыть водой из-под крана. Можно использовать мыло или 0,5-1%-ный раствор щелочи. Место ожога следует обработать дезинфицирующим раствором, лучше всего фурацилином. Обработать место ожога дезинфицирующими растворами, например, фурацилином. Если же человек выпил уксусную кислоту, тогда необходимо немедленное промывание желудка при помощи толстого зонда, который смазывается растительным маслом. В холодную воду рекомендуется добавить яичный белок или молоко. Применять слабительные средства и соду категорически запрещено. Если выполнит www.dcpt.ru |
Цельнозерновые злаковые
Цельнозерновые злаковые – это «медленные» углеводы. Тут и хлеб, и макаронные изделия, хотя бы на 50% состоящие из цельнозерновой муки, и нешлифованный коричневый рис.
Жиры
Только полезные жиры! Оливковое, рапсовое, подсолнечное и другие растительные масла подойдут для салата.
Фрукты
Употребляйте достаточно фруктов – всех цветов и размеров. Они обеспечивают вас витаминами и микроэлементами и отлично заменят десерт. |